Leica TauSTED Xtend - 時脈超解析 - 超過你的想像與預期 ...
發布日期:2024/3/29

超解析螢光奈米成像技術與系統的發展核心要素, 是基於優化成像的點擴散函數 ( PSF ), 以超解析的 [ 直接光學 ] 成像方式, 導入螢光的動態時脈, 追求 “ 超解析 - 奈米尺度的純光學解析, 實現長時間的活細胞超解析成像, 讓即時動態觀察生物有機體內的生化反應過程成為現實,為深刻認識複雜生命現象的本質打開了另一視窗,使得人們可以多層面、多視角直觀地從基因表達、蛋白質相互作用、細胞功能等有機體個體發育、遺傳進化、 重大疾病發生、環境對生命個體影響等生命現象發生、發展的過程,對闡釋生命活動的基本規律、揭 示疾病發生機理、建立疾病預警系統、提高醫療診 治水平、探尋發現新藥物具有重大作用
Leica Stellaris - TauSTED Xtend
廣域光譜式共軛焦-時脈超解析系統, 即是目前唯一的最佳解決方案 !!!

從 TauSTED Xtend 來看 : 突破探索生命科學微觀世界的新途徑
TauSTED Xtend 是開啟對 " 活體細胞的超解析奈米成像技術 " 的新視界. 如果從顯微影像技術與系統的演進發展, 我們可以依序看到 - 螢光顯微鏡 – 共軛焦顯微鏡 – 光譜共軛焦顯微鏡 – 超解析奈米螢光奈米成像 – 廣域光譜時脈共軛焦超解析奈米成像 … 這條清晰的演進道路, 已來到 TauSTED Xtend 新世代了 !!!
使用TauSTED Xtend,您將擁有更廣闊的視野。在奈米尺度的純光學解析度下擴展活細胞成像能力, 意味著您可以在奈米尺度上進行活細胞成像,並解析圖像中更小的細節。揭示亞細胞過程的秘密。TauSTED Xtend利用壽命和空間資訊來提高解析度和對比度,使您能夠以前所未有的深度研究活體或完整的標本。
TauSTED Xtend可以進行更長時間的活細胞成像, 可以進行溫和的STED成像,保護您的樣本在延長的實驗過程中不受損害。現在,您可以執行更長時間的時間延遲實驗,拍攝更多幀數和更大體積的成像,同時使用較小的光劑量來保護您的樣本。
顯微成像技術是探索生命科學微觀世界的重要途徑, 從突破探索生命科學微觀世界的障礙, 從微米到奈米尺度, 如果觀看可以廣效投入對活體細胞的成像技術發展與時程的演進, 我們發現有三個關鍵節點都有關鍵性的重大影響, 也都獲得諾貝爾化學獎 :
1). 2008年諾貝爾化學獎 - 綠色螢光蛋白 (GFP) 的發現, 開啟了應用 GFP 於活細胞與活體組織的螢光成像的可行性
綠色螢光蛋白對科學的影響,猶如當年顯微鏡的發明;這種存在水母體內的物質為後來的生物學、醫學及基因研究開啟全新研究途徑。開啟了應用 GFP 於活細胞與活體組織的螢光成像的可行性.
螢光蛋白 開啟生物醫學新頁. 透過螢光蛋白的協助,在研究生物機轉、疾病感染或癌症轉移時,不必再單靠前後生物變化,猜測當中可能的轉變及有關的基因或因子,而只要植入螢光蛋白後,就可直接觀測到轉變過程及相關機制,不但減少時間人力,也大幅提高研究的準確度。
三位諾貝爾化學獎共同得主, 分別是 :
The Nobel Prize in Chemistry 2008 was awarded jointly to Osamu Shimomura, Martin Chalfie and Roger Y. Tsien "for the discovery and development of the green fluorescent protein, GFP"

2, 2014年諾貝爾化學獎 - 超分辨螢光顯微鏡技術 ( Superresolution ) 開啟了奈米尺度應用於活細胞與活體組織的螢光成像的可行性
突破光學顯微鏡的繞射極限, 為生物學研究帶來重大的貢獻. 把光學顯微鏡 ( Microscope ) 從微米解析推進到奈米解析螢光顯微鏡 ( Nanoscope ), 三位諾貝爾化學獎得主, 分別為 : Eric Betzig、Stefan W. Hell 和William E. Moerner.
探索生命科學的作用過程,需要觀察細胞內細胞器、病毒、寄生蟲等在三維細胞空間的精確定位和分佈.另一方面,也要求闡明蛋白質結構、定位與功能的關係以及蛋白質 - 蛋白質之間發生相互作用的時空順序;生物大分子,主要是結構蛋白與 RNA 及其複合物,如何組成細胞的基本結構體系;重要的活性因子如何調節細胞的主要生命活動,如細胞增殖、細胞分化、細胞凋亡與細胞信號傳遞等.反映這些體系性質的特徵尺度都在奈米量級,遠遠超出了常規的光學顯微鏡的分辨極限 ( xy:200 nm,z:500 nm )
早在1873年,德國的物理學家阿貝,就發現了顯微鏡的光學繞射極限約在200奈米, 約是一根頭髮直徑的 1/300。雖可以通過光學顯微鏡可以觀察細胞、細菌,但是無法觀察病毒,因為病毒太小了。而且,即使它能看到細胞,要追蹤細胞裡面蛋白質分子的相互作用,也無法辦到。
傳統的電顯 (EM) 可以達到納米-原子量級的解析度,可以觀察到細胞內部囊泡、線粒體等細胞器的定位,但是由於缺乏特異性的探針標記,不適合定位單個蛋白質分子,也不適合觀察活細胞和細胞膜的動態變化過程.此外, 電顯的電子波,波長短,能量高,會殺死細胞,因此無法觀察活的生物組織, 因此,生物學家迫切希望有一種實驗顯微方法,它既具有亞微米甚至納米尺度的光學分辨本領,又可以連續監測生物大分子和細胞器微小結構的演化,而並不影響生物體系的生物活性.Leica TauSTED – Xtend 是因應此一需求而發展的技術 !!!
超解析奈米成像技術, 是基於螢光的點擴散函數的改善, 演進出各種超解析奈米成像, 包括單分子奈米成像技術 - 光啟動定位顯微技術 (photoactivated localization microscopy, PALM) 和 隨機光學重構顯微技術 (stochastic optical reconstruction microscopy, STORM) 或 基於共軛焦掃描的利用螢光的開關來提升影像解析度的方法 - STED 受激放射耗乏(stimulated emission depletion)超解析奈米成像技術.。透過這種顯微鏡的超解析奈米成像技術,可以把光學解析提升至小於 100 nm, 甚至直達到單一奈米尺度, 同時, 基於光學元件與軟體的發展, 更多的自適應光調控技術, 螢光染劑的突破, 該類技術以推展到以奈米尺度觀察活的細胞內部的奧祕,例如病毒, 或 腦神經細胞如何運作等,在生物學、醫學方面的應用,無限寬廣。
STED 是直接光學成像, 無須影像的後製運算, 今日的 STED 技術, 演進過程 - CW STED, gated STED, Pulsed STED, TauSTED, TauSTED-Xtend 已導入廣域光譜與時脈技術, 實現了活細胞與活體組織的超解析奈米成像 !!!

3). 2017 年的諾貝爾化學獎 - 低溫電子顯微鏡下的顯像技術 – Cryo EM , 開啟了奈米原子尺度應用於活體細胞組織樣本的自然狀態的 3D vEM / Cryo EM 成像的可行性
我們在此闡述此技術, 主要是強調解析的尺度進入原子尺度, 並可探索生物樣本的自然狀態 ( Cryo EM, 再推至 volume EM ) .
諾貝爾化學獎表彰他們為取得生命分子的三維影像所發展的一種有效方法。運用低溫電子顯微術,研究人員現在能將生物分子在行動中凍結並以原子的尺度描繪之,這種技術將生物化學帶入了一個新的紀元。
光學顯微鏡的解析度可以看得到蛋白質在細胞中的位置;電子顯微鏡的解析度可達 0.3 至 0.25 奈米,不只可以看到蛋白質,還可以看見裡面的結構,因此對於分子生物學的研究而言非常重要。
三位諾貝爾化學獎得主, 分別為 : 瑞士籍的 Jacques Dubochet、美國籍的 Joachim Frank 和 英國籍的Richard Henderson 共同獲獎. 強調 「低溫電子顯微鏡下的顯像技術 Cryo EM 」能將生物分子凍結以保持其自然狀態,不需使用染料或定色劑,用來研究細胞結構、病毒和蛋白質的最微小細節。
目前低溫電子顯微鏡技術的應用非常廣泛包括病毒、膜蛋白、細胞蛋白等,更在2015年被自然期刊選為「年度技術」。通過光電關聯 (CLEM) 技術, 結合共軛焦與電顯, 更是拓展更多應用的領域.
Cryo-EM 可以提供與使用 X射線晶體學 相同細節的三維高解析度的影像,這是個關鍵的里程碑。Cryo EM 技術將水變成玻璃, 玻化水 (vitrified water) – 電子束將平均地繞射,並產生均勻的背景影像。玻化方法容易使用並且只需微量的樣品,由於其快速冷卻的方式,生物分子能在行動中被凍結,使得研究者能捕捉到反應過程中一系列的影像,如此他們能取得暴露出蛋白質如何行動並與其它分子作用的動態影片。
運用 Cryo-EM 也使得我們遠較以往更容易描繪膜蛋白,它們常扮演藥物的標靶角色以及形成巨大的分子錯合物。此外, 應用Array Tomography(序列切片成像,AT)是一種能夠生成納米級解析度三維資料集的有效方法。樣品被切成數百個單獨的切片,並使用掃描電子顯微鏡對每個切片進行高解析度成像。作為一種無損方法,樣品薄片保留在成像基材上,隨後可以使用其他方法(例如螢光顯微技術或其他分析方法)展開深入研究。這種山為空間的體電顯(vEM)方法不需要特定設備,可廣泛應用於任何擁有標配掃描電子顯微鏡(SEM)和超薄切片機的實驗室。vEM 的序列切片成像的這些特性使其成為探索多種樣品(如細胞、組織和植物等)的有效方法。對於後世發展分子生物學研究有很大的貢獻。


Leica Confocal 系統多年來在 FLIM (Fluoresecence Lifetime imaging) 上都有 前瞻的發展,因此 STED 結合 FLIM 的技術,更發展出 TauSTED ,解析度更高、影像 品質也更加提升。不同於 Gated STED 只利用時間差,擷取較長 lifetime 的訊號, TauSTED 加入了FLIM 的分析,另外也排除一些 lifetime 無相關性的雜訊,有效降低 背景值,提升影像對比度。因此在較低 STED laser 的狀態下得到更好的解析度。
TauSTED Xtend 將 TauSTED 的訊號,結合 lifetime 相關的 PSF 模式,進行獨有的 lifetime 相關 deconvolution 處理。TauSTED 可使用低強度雷射達到超高解析度, TauSTED XTEND 更進一步提昇了此項能力,即使脆弱的樣本也可能進行長時間超解 析觀察,可使用更低的雷射達到更好的效果。
使用 TauSTED Xtend,除了 Leica Stellaris 共軛焦系統可以提供您最高品質的時脈共軛焦成像外, 您可以導入獨一創新的 TsuSTED Xtend 時脈超解析技術:讓你感受出
簡單使用、解析銳利、成像驚豔 !
- 可輕鬆探索樣本中更小的細節-奈米級純光學解析
- 可輕鬆進行更長時間的活細胞超解析成像
- 可以使用常規的螢光染劑,遵循您偏好的CLSM/STED實驗方法
- 即使只使用單一波長的 STED 壓制雷射, 也能擴展為多色成像
- 以奈米級直接光學解析度, 直接監測細胞生命的快速動態過程
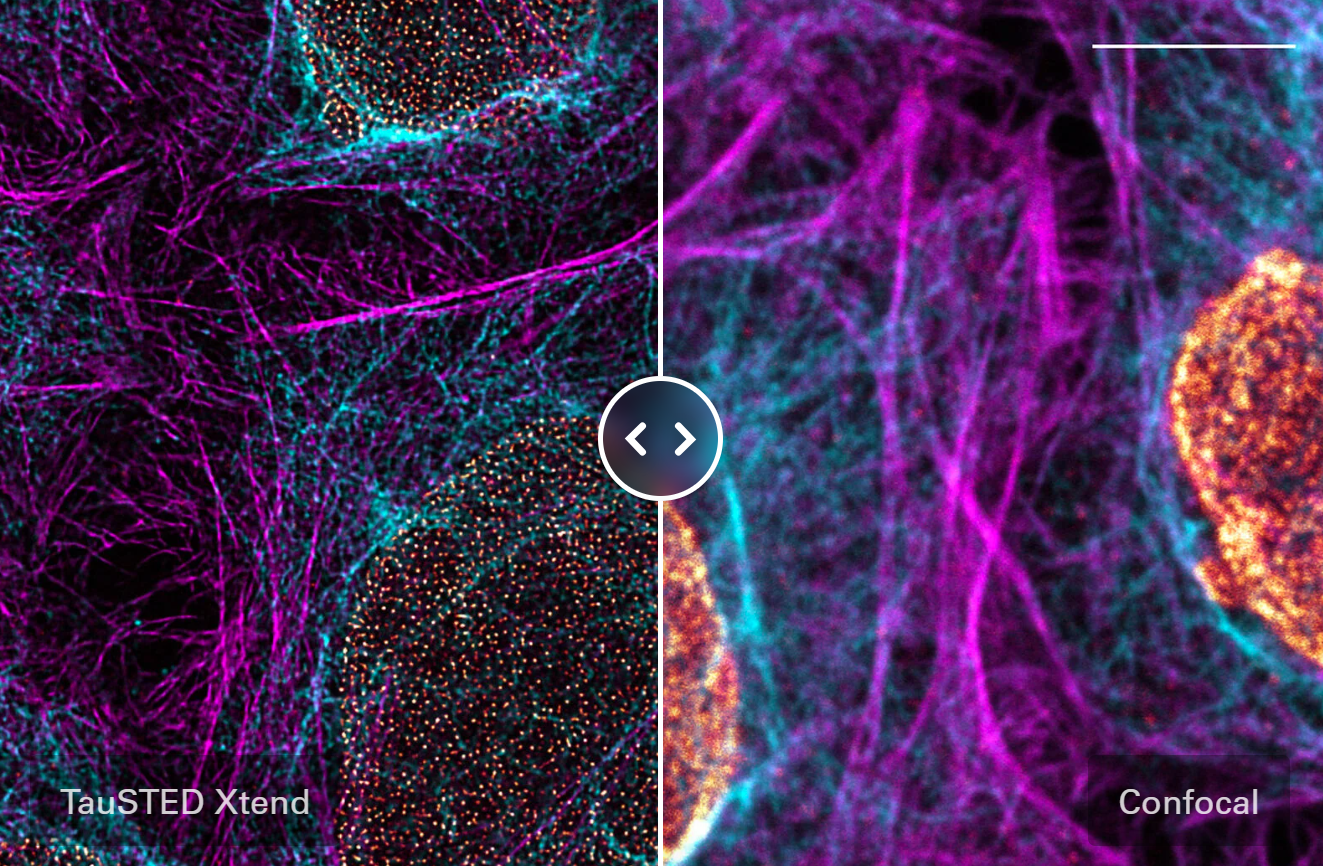
Multicolor fixed sample. TauSTED Xtend 775; Vimentin AF 594 (cyan), Phalloidin ATTO 647N (magenta) and NUP107 CF680R (glow). Image width: 39 nm. Sample courtesy of Brigitte Bergner, Mariano Gonzales Pisfil, Steffen Dietzel, Core Facility Bioimaging, Biomedical Center, Ludwig-Maximilians-University, Munich, Germany
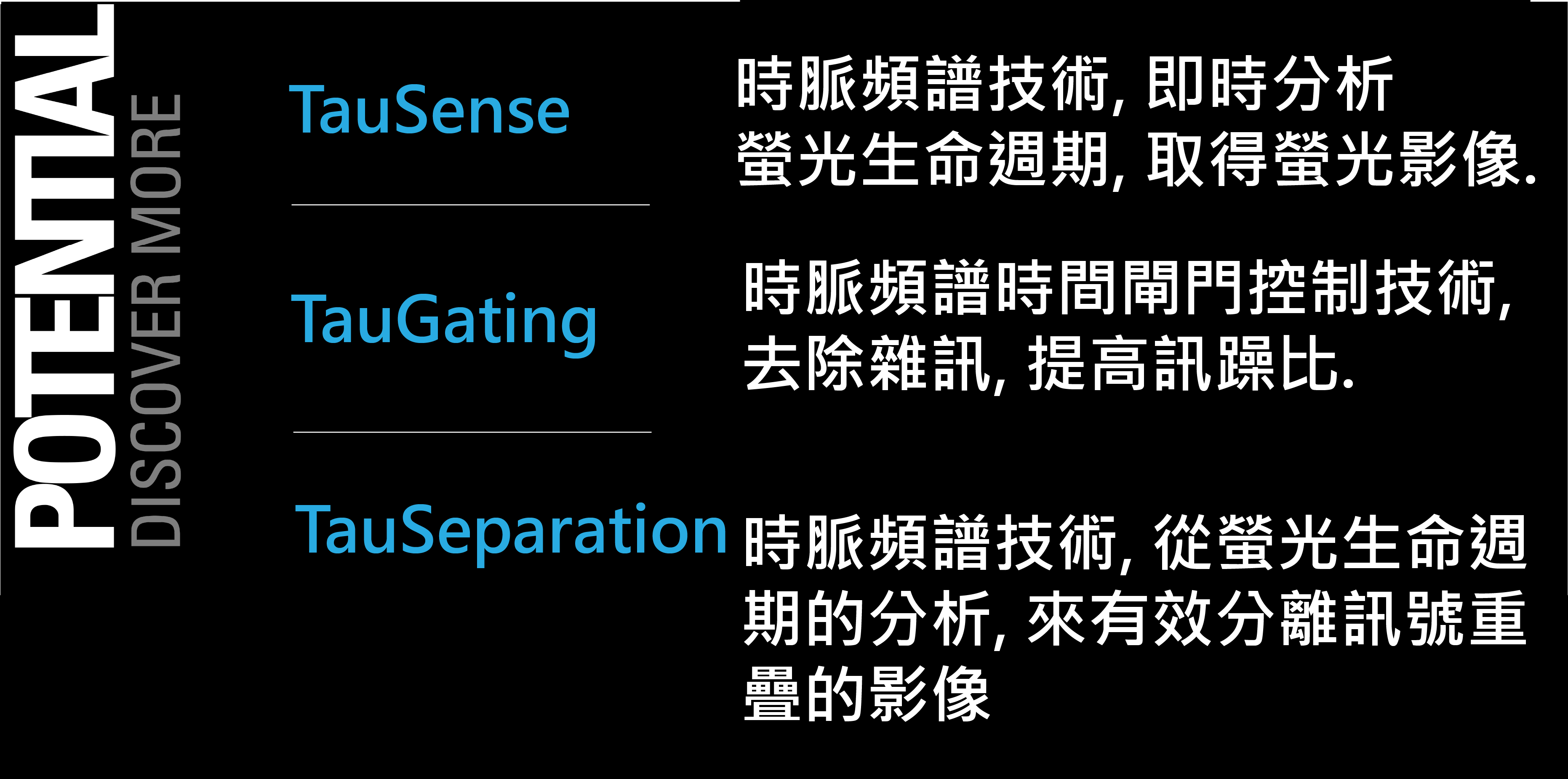
TauSense ( 時脈頻譜技術 ) 是 LEICA 的獨家創新共軛焦技術. 有別於傳統的螢光強度偵測, 它是一基於螢光壽命的高速成像技術, 是與螢光強度無關的一種對比形式。 這組成像技術包括 TauContrast、TauGating 和 TauSeparation,可以協助您瞭解細胞環境中分子的功能,提高圖像品質,擴展您可在樣本中研究的探針數量。 樣本中潛在的奧秘正在等著您去發現。
TauSTED 技術之一是每次實時測量 STED 成像中獲得的螢光壽命信息,並繪製實時相對應螢光壽命的 STED 超解析奈米即成像圖. 通過此資訊, 可讓您提高影像品質(訊號雜訊比),應用光學物理原理消除背景中的光子雜訊,無論您是使用哪一種共軛焦激發雷射波長 或 STED 壓制雷射波長(592、660、775 nm pulsed ), 最終, 都可將光學解析度因為 TsuSTED 技術, 而再度超越 傳統的基於光子強度的 STED 解析障礙限制. 最終是以直接光學方式呈現出超解析的成像結果. ( 無須再度通過耗時的影像運算與重構 ).
TauSTED Xtend 的成像系統使用了廣域光譜的脈衝式白光雷射, 與高解析的 HyD 感測器, 精準的光照控制, 使用最新進的時脈技術 (Tau) , 實現了長時間活細胞多色螢光實驗的可行性 !
TauSTED Xtend的實現, 都是以 " 自動化" 方式完成所有這一切,因此, 您可以專注於樣品, 不會錯過實驗樣本的過程與詳細信息 ! 你根本無須擔心儀器的使用設置或儀器參數的調整 !!!
STED and DNA origami imaging: TauSTED with 775 delivers resolutions <30nm on GATTA-Bead R whose nominal size is 23 nm. Scale bar: 1 µm
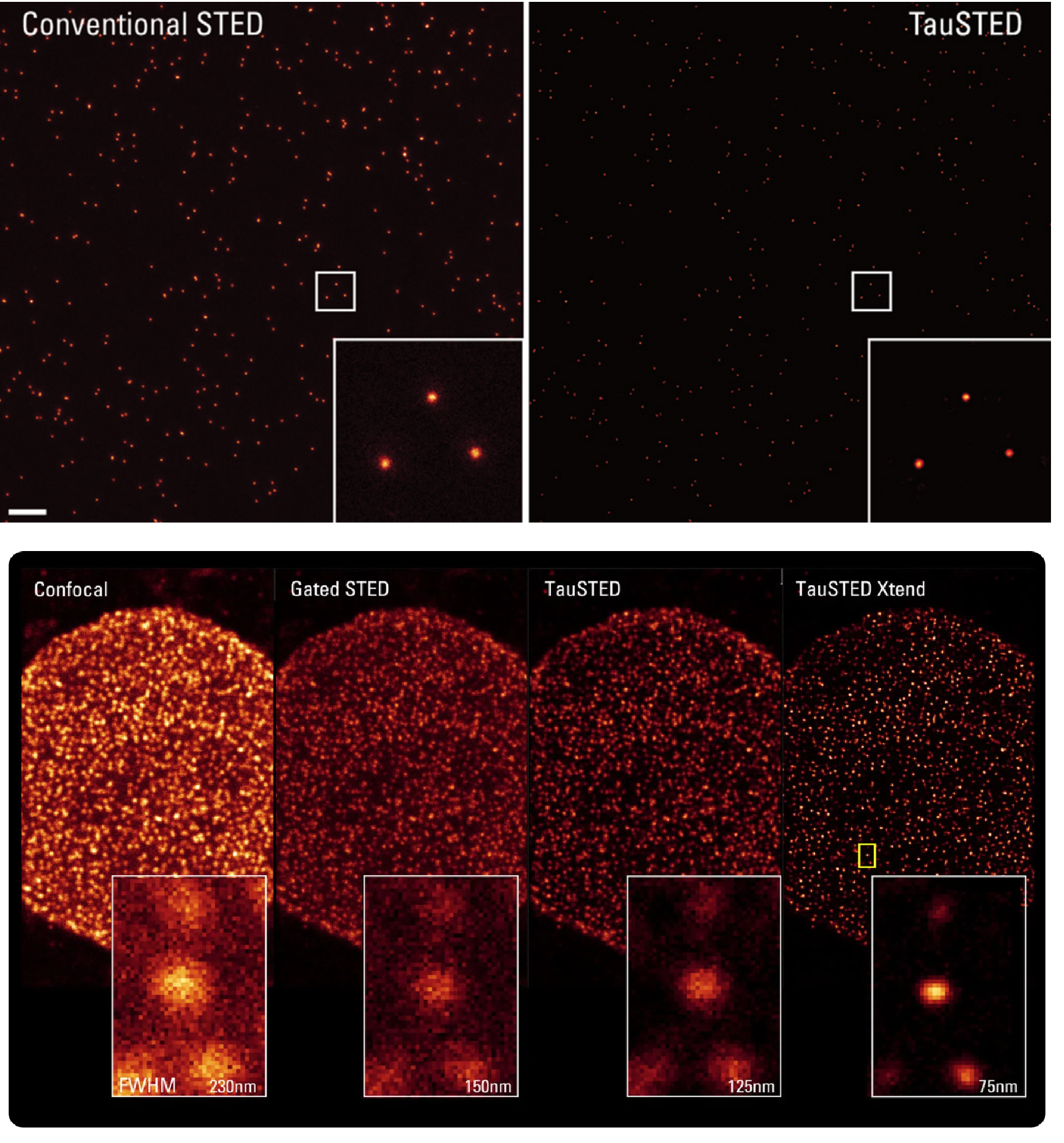 TauSTED Xtend reveals the distribution of nuclear pores (NPCs) on COS7 cells immunostained for NUP complexes with AF 488. Only 0.5% of STED light reveals much more detail.
TauSTED Xtend reveals the distribution of nuclear pores (NPCs) on COS7 cells immunostained for NUP complexes with AF 488. Only 0.5% of STED light reveals much more detail.從成像技術與系統設計的視界來論, LEICA 的 TauSTED Xtend 已是螢光影像解決方案的創新極致了 ! 傳統的間接式依靠影像運算重構的超解析技術已式微 (例如 PALM, STORM .. ), 過去一代的 Pulsed STED 欠缺 TauSTED 技術, 也難以廣泛應用在長時間的活細胞成像.
Leica 獨一的TauSTED Xtend 承襲 過去的脈衝式 STED 技術, 以嶄新的姿態, 把超解析技術發揮到極致, 最終, 已可輕易地使用在活細胞成像的應用.
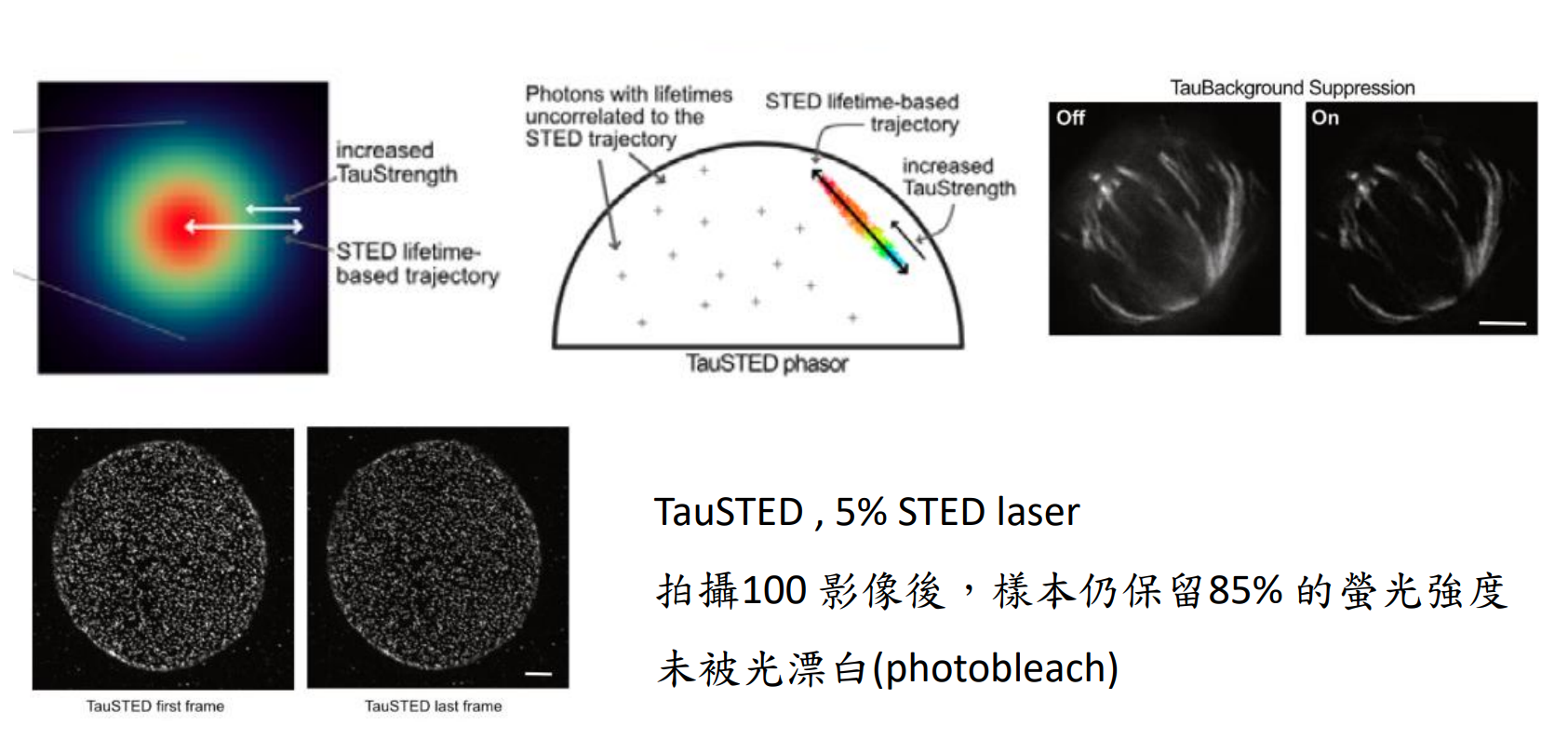
在 LEICA Stellaris 廣域光譜式共軛焦系統 的基礎上, 再延升至 TauSTED Xtend, 講得白話一點, 就是採用新的時脈技術, 在共軛焦基礎, 讓螢光成像達到奈米級的光學解析, 此, 即是新世代的超解析奈米科技, 科研人員已可以進行長時間活細胞超解析成像, 您可以探索未知的生命科學研究領域。
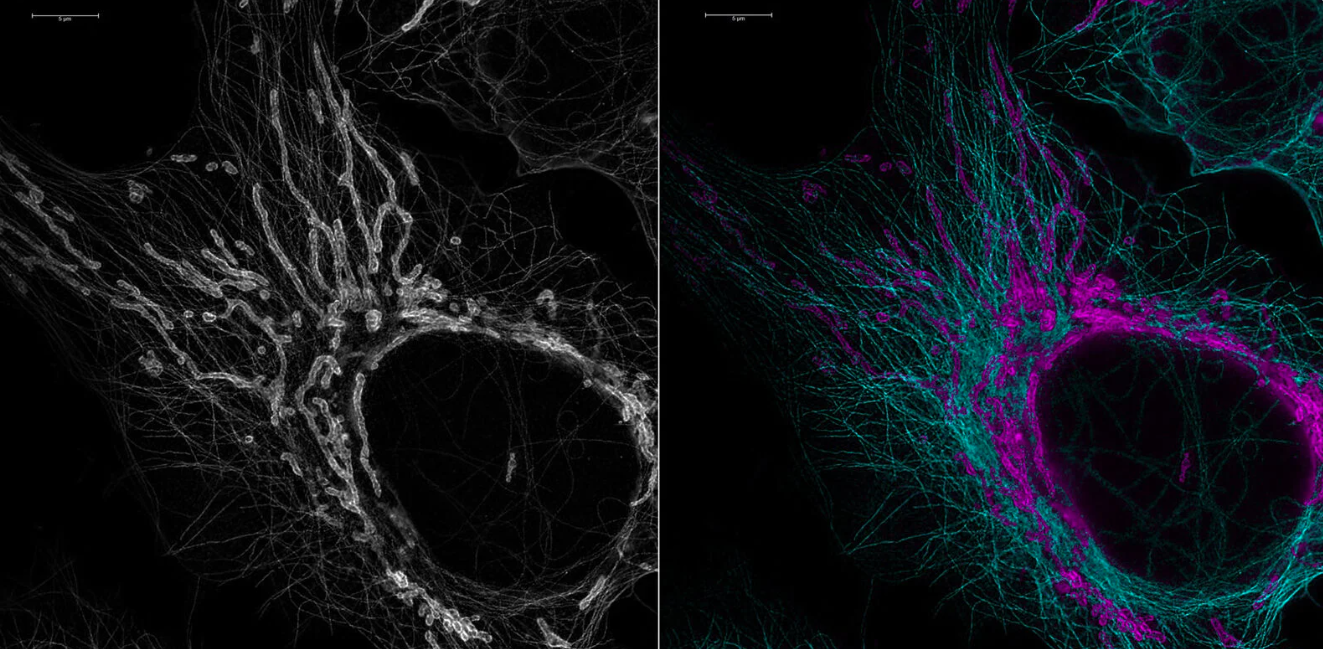
STED separation for Cell Biology: STED 775 and FALCON STED separation allow separating species with overlapping spectra using their fluorescence lifetime. In U2OS cells labeled for TOM20 and tubulin, the photon counts intensity information alone (gray) shows both structures as indistinct, while they are clearly distinguished with STED-FLIM (cyan, AF 647- tubulin; magenta ATTO 647N-TOM20).
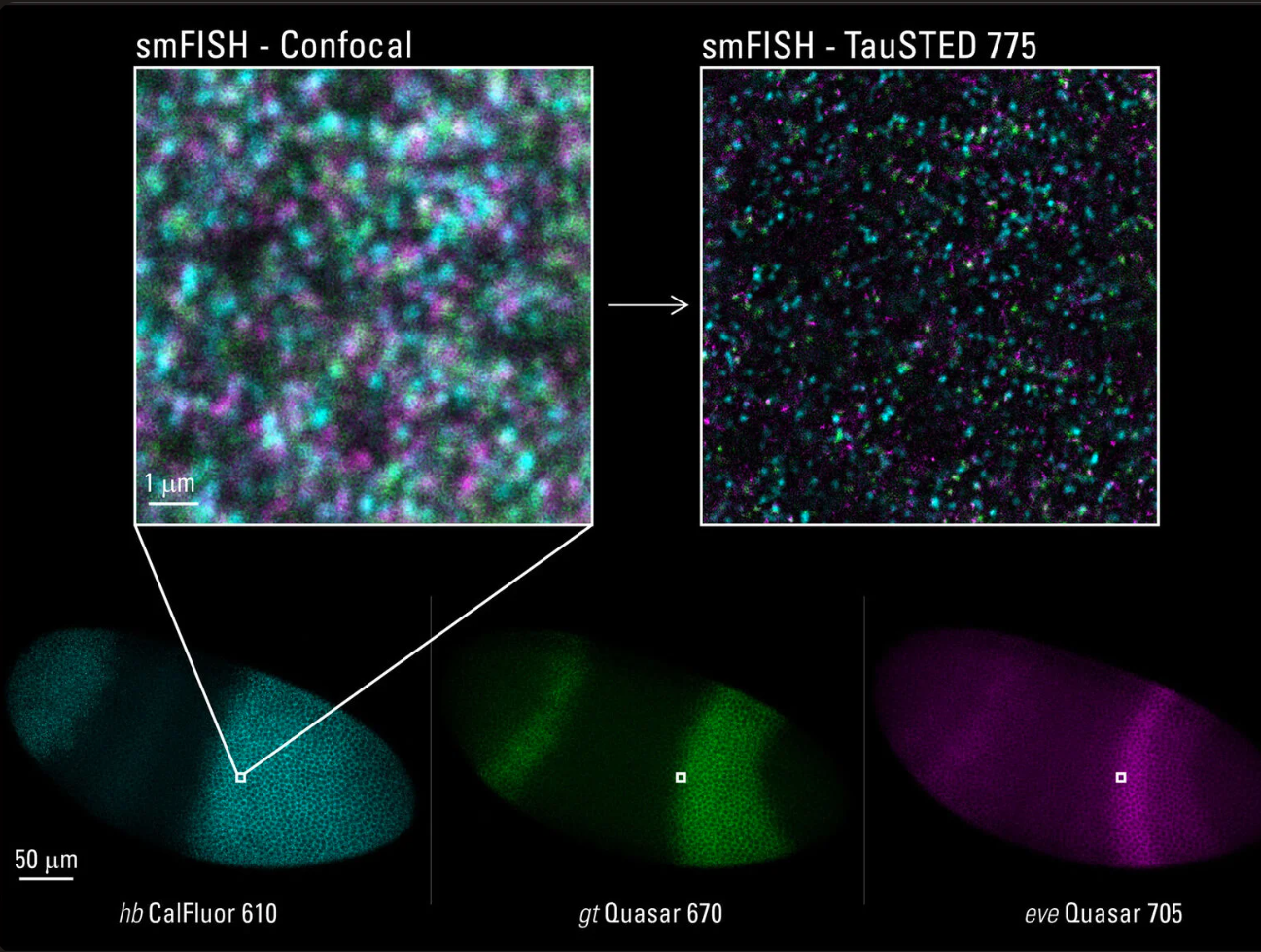
STED for Developmental Biology: smFISH* of RNA in a Drosophila embryo whole-mount preparation. Probes are directly labeled and there is no signal amplification. Top: Three color TauSTED 775 captures the signal from hb CalFluor 610 (cyan), gt Quasar 670 (green), and eve Quasar 705 (magenta). Bottom: confocal imaging of the whole Drosophila embryo. Sample courtesy of Tom Pettini, University of Manchester, UK.
*Single molecule in-situ hybridization
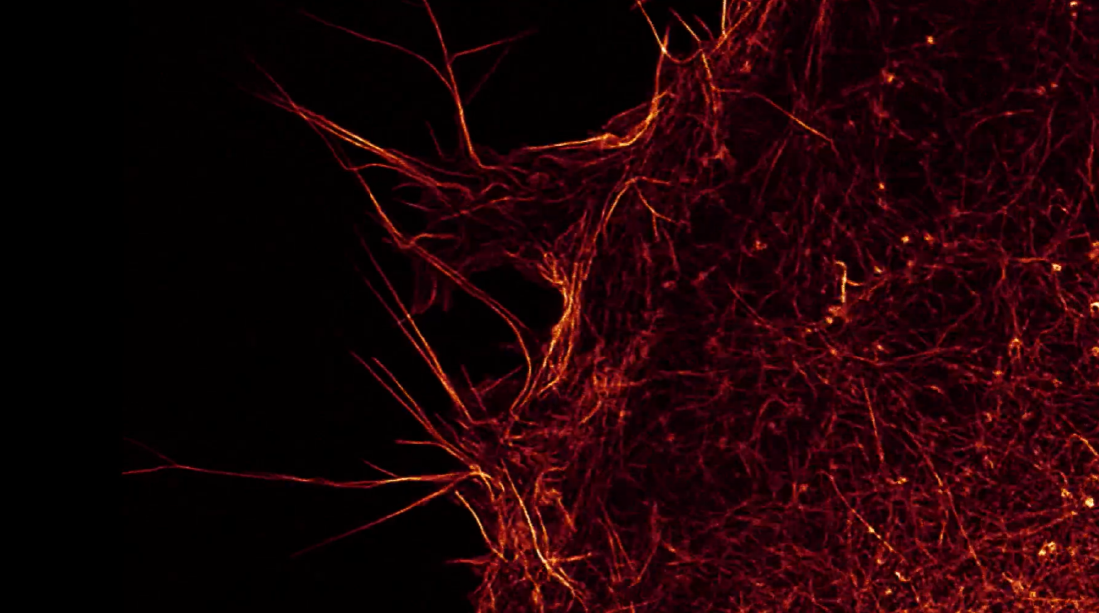
Live cells expressing LifeAct-mNeonGreen. TauSTED Xtend 589. 6 k format, 30 min STED imaging. Sample courtesy: M. Heydasch, Institute of Cell Biology, University of Bern, Switzerland.
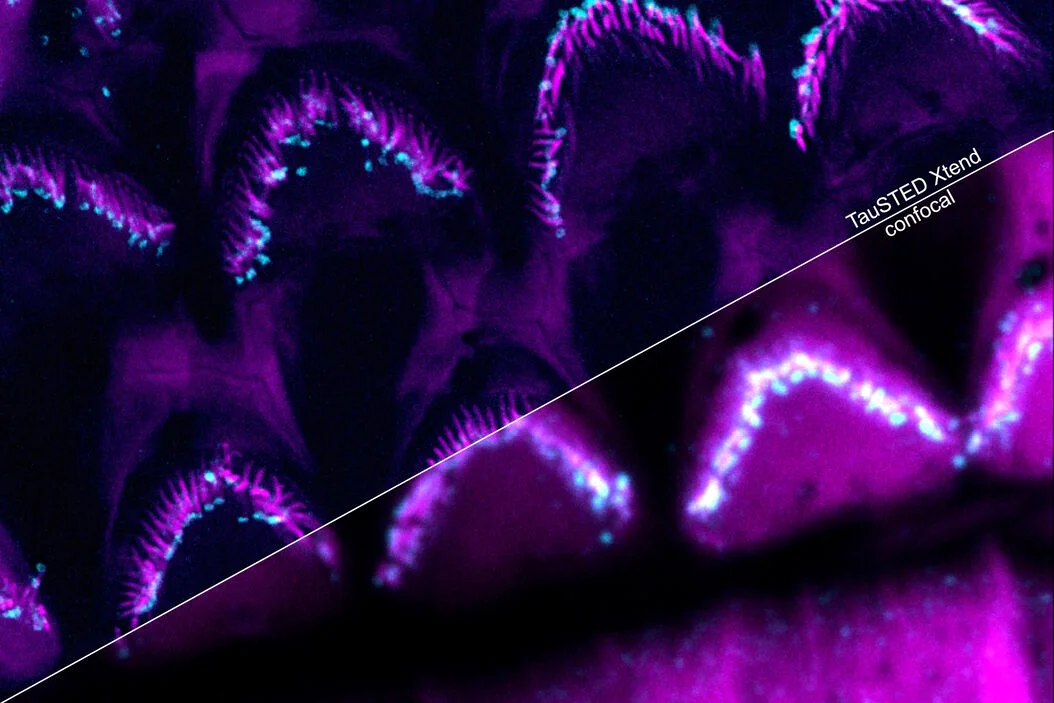
The new STED microscopy approach, TauSTED Xtend, enables extended multicolor imaging of live and intact specimen at nanoscale. By combining spatial and lifetime information, TauSTED Xtend gives access to an extra level of information that allows resolving small details in context at extremely low light dose.
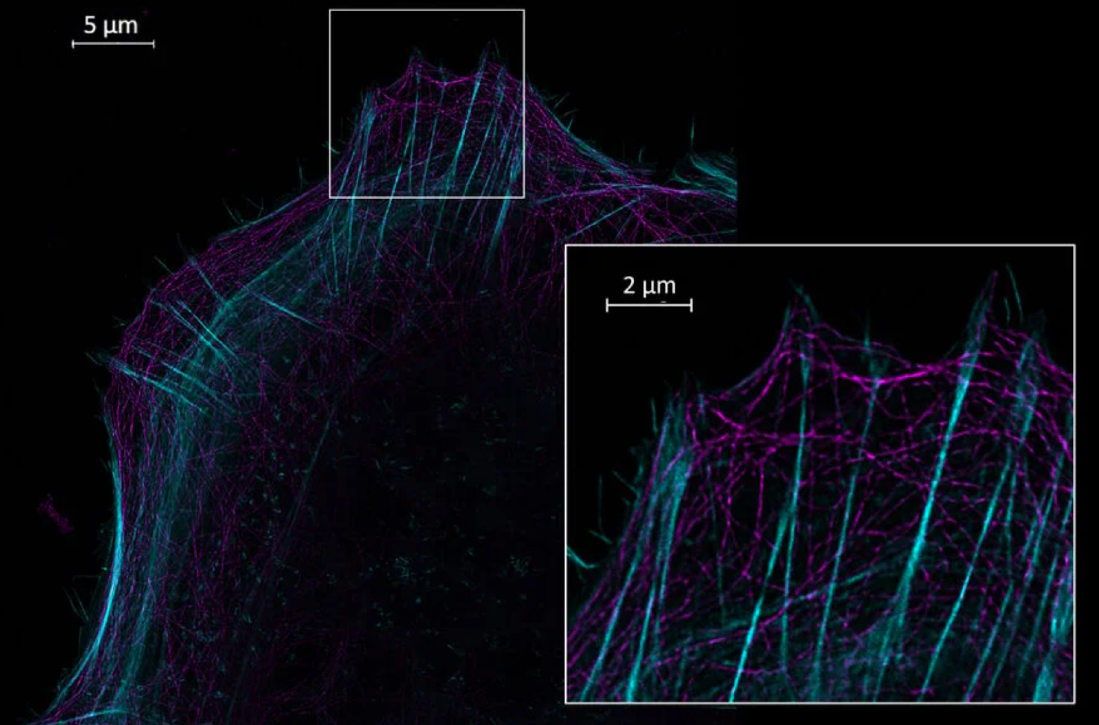
Multicolor TauSTED Xtend imaging with 589 nm STED laser using 2 standard fluorophores. CF440-Phalloidin (Actin, cyan) and StarGreen-tubulin (magenta).
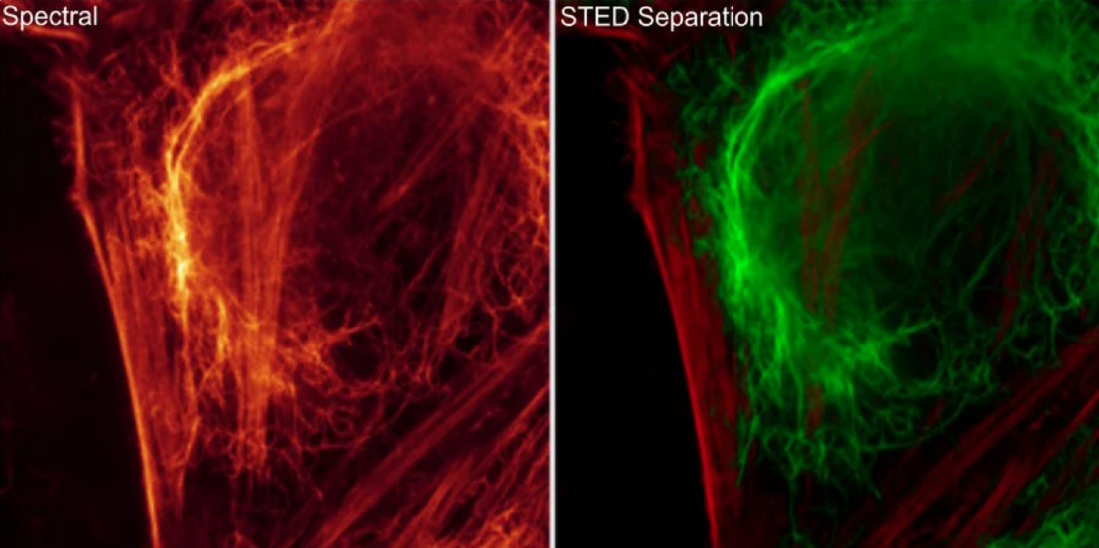
Species separation using STED Separation. HEK cells immunolabeled for Vimentin (left: green, AF 647) and stained for Actin (middle: magenta, ATTO 647N-phalloidin). Scale bar 4 mm. Sample Courtesy: S. Hänsch, S. Weidtkamp-Peters, CAI, Düsseldorf.
TauSTED Xtend 使得觀察奈米結構及其功能,及細胞動態達到前所未有的境界。 TauSTED Xtend 可在更細節和更溫和的條件下探索細胞過程和動態,促進了需要快速 變化的生物事件領域的影像上,取得了突破性的發現。這些好處適用於各種活體和 固定探針,尤其適用於 GFP(綠色螢光蛋白)。TauSTED Xtend 代表了使動態的、活 細胞超分辨顯微鏡變得更加強大和易於使用的下一步,鞏固了其作為尖端奈米顯微 鏡的首選工具的地位。通過即時觀察細胞過程的多個組成部分,可以更全面地了解 這些組成部分在細胞的複雜環境中如何相互作用。這些背景信息對於解讀細胞功能 及其在疾病中的失調至關重要。這些新的發展可能對於全面理解生物學,從健康和 疾病的機制到新治療策略的開發,都十分重要


這是一個難得的機會, 可以讓你的實驗室團隊增加先進尖端影像技術的信息, 歡迎踴躍預約簡報 !


